千億市場再掀熱浪!9款罕見病新藥上市可期,華東、諾華蓄勢待發,42個品種“解鎖”新用法
發布日期:2024-04-02 閱讀次數:575 來源:米內網原創
摘要:罕見病“用藥短缺”備受關注。近年來國家頻頻出臺利好政策,以推動罕見病新藥研發及市場準入。據不完全統計,2024年以來,至少有5款罕見病新藥登場亮相,涵蓋血液、皮膚、消化系統等治療領域;9款新品有望于年內獲批,涉及華東、諾華等知名藥企。臨床用藥需求的激增,催生超說明書用藥的規范化和普遍化,42個罕見血液病治療藥“解鎖”新用法,人免疫球蛋白注射劑、利妥昔單抗注射劑等多款2022年在中國三大終端六大市場
罕見病“用藥短缺”備受關注。近年來國家頻頻出臺利好政策,以推動罕見病新藥研發及市場準入。據不完全統計,2024年以來,至少有5款罕見病新藥登場亮相,涵蓋血液、皮膚、消化系統等治療領域;9款新品有望于年內獲批,涉及華東、諾華等知名藥企。臨床用藥需求的激增,催生超說明書用藥的規范化和普遍化,42個罕見血液病治療藥“解鎖”新用法,人免疫球蛋白注射劑、利妥昔單抗注射劑等多款2022年在中國三大終端六大市場(統計范圍見文末)銷售額超30億元的重磅品種在列。
激勵政策層出不窮,千億罕見病藥市場再起波瀾
“無藥可用”是大多數罕見病患者的常態。據統計,目前全球共發現7000多種罕見病,有藥可治的比例不足10%。我國有2000多萬罕見病患者,每年新增患者超20萬。確診難、治療方法少、可用藥品少等難題交織,讓罕見病群體身陷困境。
近年來,隨著罕見病藥進保提速,罕見病目錄相繼發布,驅動罕見病新藥研發及市場準入的利好政策陸續出臺,疊加罕見病領域未被滿足的需求大、市場競爭小等特點,越來越多企業加碼布局罕見病藥物的研發。一些“無藥可治”的罕見病患者,或能在與時間的生死賽跑中等來“救命良藥”。
近年來國家發布的部分鼓勵罕見病藥研發和生產的相關政策
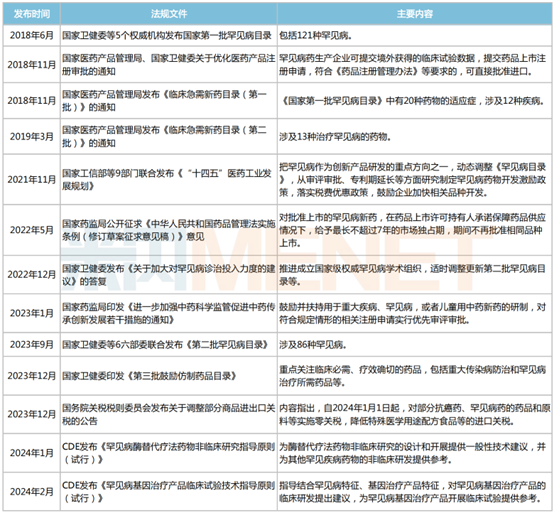
《2023年度藥品審評報告》顯示,2023年國家藥監局共批準45個罕見病藥(不含化藥4類罕見病藥),獲批產品涵蓋血液、神經、代謝、免疫、罕見腫瘤等多個治療領域,填補了我國多個罕見病的臨床用藥空白。如2023年4月獲批上市的硫酸氫司美替尼膠囊,成為首個獲批的Ⅰ型神經纖維瘤病(NF1)相關叢狀神經纖維瘤(PN)治療藥;同年6月獲批上市的卡谷氨酸分散片,用于N-乙酰谷氨酸合成酶缺乏癥(NAGSD)、丙酸血癥(PA)等引起的高氨血癥,是我國首個獲批用于該類疾病的治療藥物。
從審評審批路徑上看,共有15個品種通過優先審評審批程序得以加快上市,其中納魯索拜單抗注射液為石藥集團的1類創新藥,是全球首個IgG4 RANKL抑制劑,用于治療不可手術切除或手術切除可能導致嚴重功能障礙的骨巨細胞瘤。與原有治療藥(地舒單抗)開展頭對頭研究顯示,納魯索拜單抗具有顯著臨床優勢,米內網數據顯示,2022年在中國三大終端六大市場地舒單抗合計銷售額超過8億元,同比增長110.94%。
2023年通過優先審評審批程序獲批的罕見病藥
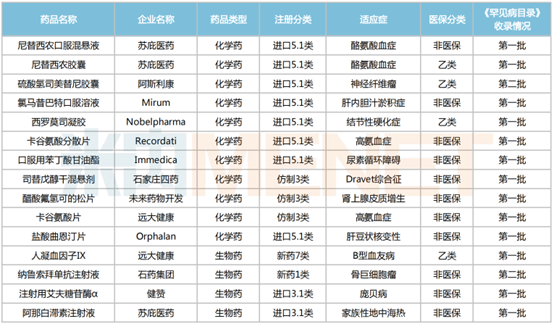
伴隨臨床用藥需求的推動,以及激勵創新研發政策的出臺,罕見病藥物市場持續升溫。有業內專業機構指出,中國罕見病藥市場于2016年及2020年分別占全球罕見病市場的0.4%及1%,預計2030年將激增至259億美元,約合1872億元(按實時匯率換算),市場潛力十足。
9款罕見病新藥上市可期,華東、諾華......蓄勢待發
據不完全統計,今年以來已有5款罕見病新藥獲批上市,包括C5抑制劑可伐利單抗注射液、銅吸收抑制劑醋酸鋅片、GLP-2類似物替度格魯肽、重組豬FⅧ(rpFⅧ)藥物注射用舒索凝血素α和IL-36R抑制劑佩索利單抗注射液。這些產品的到來,將為陣發性睡眠性血紅蛋白尿癥、肝豆狀核變性、短腸綜合征、獲得性血友病A、泛發性膿皰型銀屑病等罕見病患者帶來了新的治療選擇。
展望2024年,還有哪些備受關注的罕見病新藥在國內登場亮相,惠及更多患者?筆者結合公開資料及CDE優先審評公示信息,篩選出9款有望于今年獲批上市的罕見病新藥,以供大家參考。
2024年有望獲批的罕見病新藥
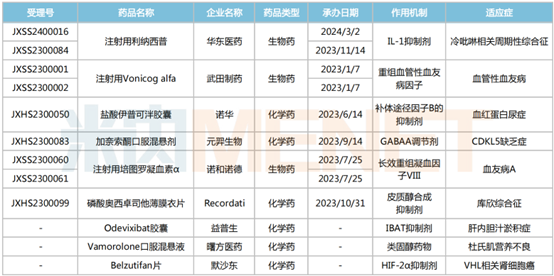
注射用利納西普由華東醫藥與Kiniksa Pharmaceuticals合作研發,是一款IL-1免疫抑制劑。米內網數據顯示,2022年中國三大終端六大市場免疫抑制劑市場規模超過280億元,2023年上半年突破155億元,全年銷售額有望再創新高。
近年來中國三大終端六大市場免疫抑制劑銷售趨勢(單位:萬元)
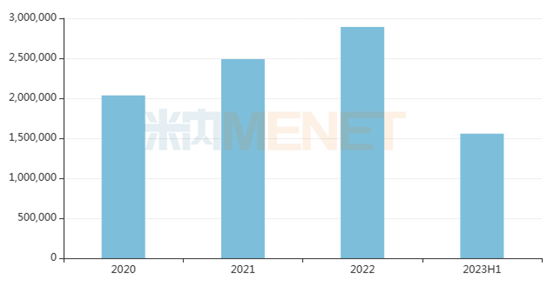
CDE官網顯示,2023年1月和12月,該藥相繼被CDE納入優先審評,分別針對成人和12歲及以上青少年冷吡啉相關周期性綜合征(CAPS)、成人和12歲及以上青少年復發性心包炎(RP)。
目前,國內暫無用于冷吡啉相關周期性綜合征,以及復發性心包炎的有效治療藥物。2018年11月,注射用利納西普被納入CDE發布的《臨床急需境外新藥名單(第一批)》;2023年9月,CAPS及復發性心包炎均被收錄于國家衛健委發布的《第二批罕見病目錄》。
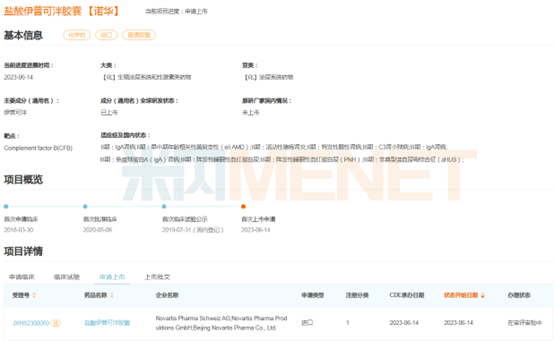
鹽酸伊普可泮膠囊是諾華研發的一款靶向補體旁路途徑B因子的口服抑制劑。2023年6月,該藥的上市申請被CDE納入優先審評,用于治療成人陣發性睡眠性血紅蛋白尿癥(PNH)患者。
靶向抑制補體C5是PNH的標準療法,米內網數據顯示,目前全球僅有2款針對PNH治療的C5抑制劑獲批上市,其中阿斯利康的依庫珠單抗已在國內獲批。現有的C5抑制劑以輸注的方式給藥,且可能無法控制PNH癥狀,部分患者在接受抗C5治療后仍有殘存貧血和依賴輸血。
而鹽酸伊普可泮膠囊是一種B因子抑制劑,B因子驅動了PNH中補體介導的溶血。該藥通過作用免疫系統的補體旁路途徑中的近端通路,可全面控制血管內外的紅細胞破壞(血管內和血管外溶血)。該藥已于2023年12月獲FDA批準,作為口服單藥療法治療成人PNH。
鹽酸伊普可泮膠囊項目進度
注射用Vonicog alfa是武田研發的一款重組血管性血友病因子。2023年1月,該產品的上市申請被CDE納入優先審評,適應癥為成人血管性血友病(VWD)患者,包括按需治療和出血事件的控制,以及圍手術期出血管理。
血管性血友病為常見的遺傳性出血性疾病之一,是因血管性血友病因子(VWF)基因突變引起血漿中的血管性血友病因子數量減少或質量異常所引起的疾病。注射用Vonicog alfa包含完整的VWF多聚體,含有超大多聚體(ULMs),半衰期長,可有效實現血管性血友病的替代治療,并為患者提供個性化的出血控制方法。
據悉,該藥是全球首個且唯一一個重組血管性血友病因子產品,目前已在美國、歐盟、加拿大、瑞士、澳大利亞和日本等地獲得上市許可,用于18歲及以上血管性血友病患者的按需治療和出血事件控制,以及圍手術期出血管理。
注射用Vonicog alfa全球獲批及申報上市情況

42個品種“解鎖”新用法,多款超30億重磅產品在列
除了加快罕見病藥上市步伐,針對罕見病用藥可及性低等問題,廣東省藥學會于近日發布了《血液系統罕見病超藥品說明書用藥專家共識(2024版)》(下文簡稱《共識》),有望進一步提高部分罕見血液病獲得治療的可能性。
據梳理,《共識》由廣東省藥學會罕見病專家委員會組織編寫,從12種血液系統罕見病共42種治療藥物遴選出62條用藥方案凝結而成。
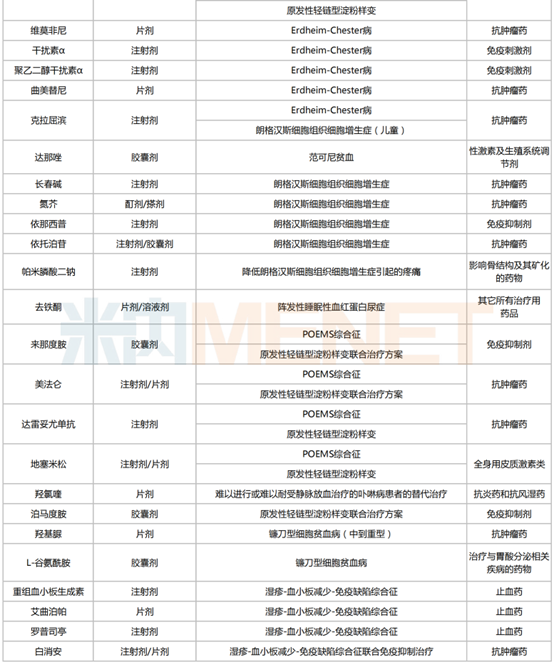
從超說明書內容上看,新增針對血友病及其相關疾病治療的用藥信息最多,合計11條;用于朗格漢斯細胞組織細胞增生癥(8條)、原發性輕鏈型淀粉樣變(8條)、Castleman綜合癥(7條)、Erdheim-Chester病(7條)、濕疹-血小板減少-免疫缺陷綜合征(7條)等位居其后。
具體產品情況方面,超說明書適應癥達3項及以上的品種有5個,分別為潑尼松片劑、環磷酰胺注射劑/片劑、環孢素注射劑/膠囊劑/溶液劑、沙利度胺片劑以及硼替佐米注射劑。從治療亞類上看,抗腫瘤藥為主力,占據14個席位;免疫抑制劑、止血藥分別占9個和8個,免疫刺激劑和全身用皮質激素類則各占2個。
罕見病藥超說明書用藥專家共識(血液系統-2024版)

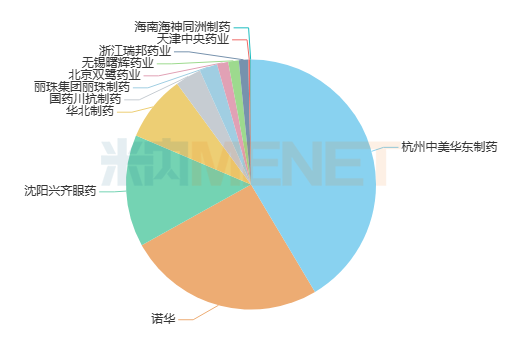
環孢素是由11個氨基酸殘基組成的環狀多肽藥物,主要用于器官移植后的免疫抑制、銀屑病、腎病綜合征等。在中國公立醫療機構終端,該品種2022年銷售額超過20億元,2023年上半年同比增長7.01%,中美華東制藥、諾華、興齊眼藥市占比均達兩位數。在本版《共識》中,環孢素新增了3項超說明書適應癥,包括獲得性血友病免疫抑制治療、Castleman綜合癥及朗格漢斯細胞組織細胞增生癥,將為罕見血液病患者提供了新的用藥選擇。
2023年上半年中國公立醫療機構終端環孢素品牌格局
硼替佐米是雙肽基硼酸鹽類似物,是全球首款人工合成的新型蛋白酶體競爭性抑制劑,主要用于多發性骨髓瘤和套細胞淋巴瘤的治療。受國采影響,該品種在中國公立醫療機構終端銷售額逐年下滑,從2020年的超17億元跌至2022年的約6億元。在本版《共識》中,硼替佐米被允許超說明書用于血液疾病治療領域,涉及Castleman綜合癥、POEMS綜合征、原發性輕鏈型淀粉樣變等,有望拉動其銷售市場的復蘇。
42個納入本版《共識》的品種中,還包括人免疫球蛋白注射劑、利妥昔單抗注射劑、重組血小板生成素注射劑、嗎替麥考酚酯注射劑/片劑/膠囊劑等2022年在中國三大終端六大市場銷售規模超30億元的重磅藥,產品潛力有望進一步釋放。
相關新聞

“釔”朵小紅花:尋找治愈希望 傳遞生命力量
9369個小時之前

2024 ASCO恒瑞醫藥14款創新藥共79項抗腫瘤領域研究成果登場亮相
9441個小時之前

《近視防治指南(2024年版)》明確,眼保健操、OK鏡、低濃度阿托品滴眼液可延緩近視
5月31日,國家衛生健康委印發《近視防治指南(2024年版)》,進一步提高近視防控和診療的規范化水平,推動和加強我國近視防治工作。
9441個小時之前

Molecular Cancer | 邁向癌癥治療新紀元:CAR-M療法的臨床潛力
近年來,嵌合抗原受體(CAR)技術在血液腫瘤治療中取得了顯著進展,特別是在急性淋巴細胞白血病(ALL)、淋巴瘤和漿細胞骨髓瘤(PCM)等方面。然而,CAR-T細胞療法在實體瘤治療中的效果仍不盡如人意。這促使研究人員開始探索替代性的免疫治療方法,以克服當前CAR-T細胞面臨的重大挑戰。具有強大吞噬能力、抗原呈遞功能以及能夠調節腫瘤微環境和刺激適應性反應的巨噬細胞成為一種有前景的選擇。
9441個小時之前

以標準化引領國產手術機器人產業高質量發展
隨著醫療技術的飛速發展,手術機器人作為醫用機器人領域的重要分支,憑借有效提高手術效率、降低人力成本等顯著優勢,正受到醫療器械行業越來越多的關注。為了促進手術機器人領域創新產品加速上市,提高產品質量安全水平,保障醫護人員及患者用械安全,我國藥監部門積極推進醫用手術機器人標準體系不斷完善,手術機器人標準化工作取得積極進展。
9538個小時之前













